文章作者:华赢证券
2024年8月6日,拟在港上市的国际临床眼科医药公司拨康视云Cloudbreak Pharma(以下简称“拨康视云”)宣布,与日本药企参天制药株式会社(以下简称“参天制药”)签署合作协议,将其正在研发的用于翼状胬肉治疗的多激酶抑制剂CBT-001,授权于参天制药,该授权涉及日本、韩国、越南、泰国、马来西亚、菲律宾、新加坡和印度尼西亚在内的东南亚地区(以下简称“地区”)。根据协议条款,拨康视云授权参天制药在该地区开发、生产和商业化CBT-001药品。

根据协定,拨康视云将获得总额高达9,100万美元的首付款及里程碑付款。此外,拨康视云还将获得产品未来净销售额的两位数百分比,作为该产品的特许权使用费。
拨康视云去年11月底向联交所提交申请,拟于主板上市,申请六个月有效期过去后,再于今年5月重续申请,联席保荐人为瑞银、建银国际及华泰国际。去年曾有市场消息指,拨康视云计划在港上市集资2亿美元。集资所得预期用于核心产品CBT-001的持续临床研发活动、拨付持续临床研发活动,以及建设生产设施和商业化活动等用途。

拨康视云于2015年在美国成立,创始人兼首席执行官倪劲松博士在药物发现和药物开发方面拥有超过二十年的制药行业和学术研究经验。在创立拨康视云之前,倪劲松博士曾在Allergan担任科学总监15年,并在辉瑞担任高级科学家3年。在Allergan和辉瑞任职期间,倪劲松博士就一直专注眼科和皮肤科疾病,并领导项目团队成员成功推出了多款相关产品。
自2015年成立以来,拨康视云持续深耕眼科创新药领域。公司以美国加州为起点,逐步构建起全球化的研发与产业布局后,继而在广州与苏州设立分支机构,持续拓展研发和生产能力。拨康视云专注于产品的自主研发与差异化创新,目前已有多项成果达到了国际首创的新适应症与机理,致力于成为First-in-Class眼科创新药领域的先驱。
最新初步招股资料显示,由于还没有药物被批准用于商业销售,拨康视云仍未有任何销售收入,再加上受研发等因素的影响,这家公司在2022年至2023年的报告期,净亏损也从0.67亿美元增加到1.29亿美元。
从2022年的0.15亿美元,到2023年的0.28亿美元,拨康视云在研发上的大力投入,也使得自身在全球拥有51项获授专利及140份待授专利申请。其中,CBT-001在全球有41项获授专利及62项待授专利申请。
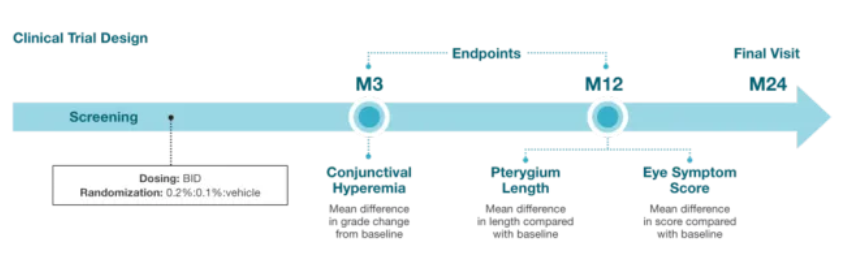
目前专注于研发7种药物,其中CBT-001是拨康视云研发的一种乳化型尼达尼布滴眼液,主要用于治疗翼状胬肉(一种眼表非恶性的纤维血管组织异常增生)。尼达尼布是一种多激酶抑制剂,主要用于VEGF(血管内皮生长因子)受体、PDGF(血小板衍生生长因子)受体和FGF(成纤维细胞生长因子)受体,从而抑制血管新生和纤维化。CBT-001在美国完成了II期临床试验,目前正在美国、中国、澳洲、新西兰和印度开展大规模的全球多中心III期临床试验。CBT-001能通过滴眼液的方式为医生和患者提供一种新的翼状胬肉治疗选择,抑制病情发展。若成功推出市场,将是市面上首只治疗眼翳的药物,另亦有数款药物处于临床阶段。
翼状胬肉是一种眼表的非恶性的纤维血管组织异常增生,增生从球结膜开始并延伸至角膜表面。翼状胬肉具有侵入性的生长趋势,且具有复发倾向和非转移性。尽管翼状胬肉是非恶性的,但它可能引起明显的眼部症状,包括充血、刺激、疼痛和异物感,从而影响患者的生活。
目前,市场上尚无批准的治疗翼状胬肉药物,医生通常会使用未有临床试验认可的人工泪液和短期局部眼用类固醇当作处方。然而,这些药物在长期使用中可能无效或不安全。当翼状胬肉侵入视轴或者持续充血时,通常需要进行手术切除。虽然有多种手术方法,如转位术和结膜瓣移植,但所有方法都有复发的倾向,这被视为翼状胬肉手术中的问题。
由于紫外线与这种疾病的病发和进展相关,翼状胬肉患者最常见于低纬度的阳光充沛地区。有研究表明,全球约10%的人口受此影响,在日本约有400万患者。在日本,40岁以上人群中翼状胬肉的患病率估计为4%,该人群在韩国为3.8%,在越南、马来西亚、菲律宾和泰国为10.1%。
据拨康视云招股书,全球治疗翼状胬肉药物的市场规模预计将于2027年达到2.73亿美元,于2032年达到25.29亿美元,复合年增长率为56.0%。美国治疗翼状胬肉药物的市场规模预计于2027年达到13.59百万美元及于2032年达到14.17亿万美元,复合年增长率为59.8%。中国治疗翼状胬肉药物的市场规模预计于2027年达到2.18亿美元,于2032年达到20.22亿美元,复合年增长率为56.1%。
这也意味着,拥有CBT-001的拨康视云,已经在治疗翼状胬肉药物的市场中占据了先机。







